eTMF临床研究主文档管理系统
据调研,eTMF临床研究主文档管理系统,是继EDC及CTMS之后使用最为广泛的临床研究信息化系统,是为临床研究高度定制的成熟临床试验文档管理解决方案。作为临床研究过程一体化的重要元素,能帮助企业及时、合规、安全有效地收集管理文档。
临床研究电子化注册申报时代来临
日前,CDE就eCTD格式申报发布了《eCTD技术规范(征求意见稿)》和《eCTD验证标准(征求意见稿)》,整体技术规范可以说是参照欧美标准,这标志着我国临床研究注册申报又向国际化和信息化迈进了一大步。临床试验纸质文档存档时代将逐渐告别,信息化系统、流程和数据的结合与运用将成为关键,在各个环节发挥重要作用。
然而,对于企业来说,向电子化递交的转型,面临着从递交文件格式规范化、结构规范化以及内容规范化等一系列挑战,同时eCTD专业人才的缺乏,很有可能使得企业加剧递交风险。
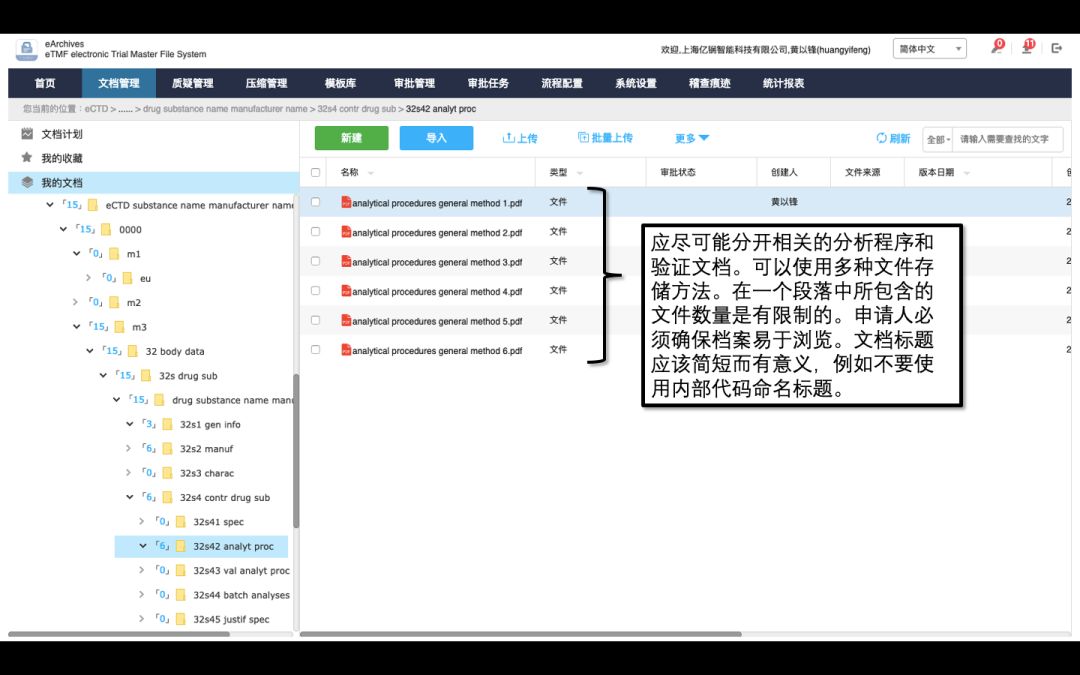
eTMF对于文档格式和结构设置的高度规范化,可以帮助企业完成eCTD的格式管理,通过eTMF可以规范文件目录、限制文档格式,大大减少收集后期对于文件的整理和校验。
太美医疗科技于2014年推出第一版eTMF系统,并命名为eArchives。经过几年的优化升级,产品功能不断完善与成熟,产品性能不断加强、操作体验不断优化,得到越来越多使用者的认可。
罗氏诊断、复星医药、深圳微芯、广州博济、康德弘翼等知名制药企业和CRO公司已经选择使用 “eArchives” 作为企业临床试验文档标准,建立企业临床试验文档管理体系。
eArchives实时管理执行临床试验过程中的所有TMF文档和进程。这一信息化管理TMF的运作模式加强收集TMF的质量及效率。
管理者可以通过eArchives随时了解TMF整体状况,及时发现问题并质控,提高企业临床试验质量并降低风险。
使用者能够通过eArchives随时更新、质控、内部稽查TMF,解决以往固有的TMF管理顽疾,形成标准作业程序,如:
多中心多人员多地域分布:提供长期稳定收集和管理文件的计划和操作方法
文件管理SOP难以有效遵循:eArchives配合SOP建立质控流程,形成追踪、反馈、纠正的闭环机制
人员流动大且能力参差不齐:eArchives辅助新进人员规范化管理文件
纸质储存文件缺失:eArchives提供文件完整性质控和安全备份机制
更重要的是,在太美医疗科技搭建的医药研发协作平台上,拥有eCooperate(CTMS)、eArchives(eTMF)和eCollect(EDC)、eImage(医学影像阅片系统)、eBalance(随机系统)、eReport(患者报告结果系统)、eSafety(药物警戒系统)、eSite(机构管理系统)、eTrial(一期病房系统)等覆盖临床研究全程的软件产品,帮助临床研究运营和管理以及数据共享与存储,形成完整信息化流程。

联系我们,了解更多eArchives和太美医疗科技相关信息








